KORROSION WISSEN ÜBERSICHT
Was ist Korrosion?
Das Wort Korrosion stammt aus dem lateinischen und heisst in der Bedeutung „zerfressen“. Der Stahl wird zerfressen und das Ergebnis sind schwere Schäden und teure Reparaturen, die jedes Jahr der Gesellschaft eine Menge Geld kostet. Wissenschaftlich betrachtet handelt es sich bei der Korrosion um das elektrochemische Auflösen von Metallen. Bei diesen Prozess oxidieren Metalle von Blechen und Rohren, bis nur noch unbrauchbarer, verrosteter Schrott übrig ist, d.h. das Material verliert die Form und wird seiner Aufgaben nicht mehr gerecht.
Wir arbeiten an dieser Webseite! Dies sind lediglich einige Textbeispiele um das Thema Korrosion. Wir würden uns sehr über Ihre Mitwirkung in Form Text und Bildmaterial freuen und darüber Ihre Webseite direkt verlinken.
Korrosion entsteht in Abhängigkeit von 3 Voraussetzungen:
1. Auftreten von Feuchtigkeit.
Ohne Feuchtigkeit keine Korrosion!
Häufige Ursachen für Wassereinwirkungen sind Wasserdampftransport, Reinigungswasser, Undichtigkeiten der Anlage, Regenwasser und Sprühflutanlagen. Die Korrosionsrate unter feucht gewordener Dämmung liegt zwanzigfach höher als bei Umgebungsbedingungen.
2. Die chemische Zusammensetzung von Wasser
kann bei Edelstahl und nichtrostenden austenitischen Stählen Korrosion hervorrufen.
Saure Bestandteile aus örtlicher Luftverschmutzung können sich am Metall anlagern und Dämmstoffe setzen auch Säuren und Salze frei.
3. Betriebstemperatur der technischen Anlage
Bei Betriebstemperaturen zwischen 0 °C und 100 °C ist Wasser im flüssigen Aggregatzustand. Unter diesen Bedingungen verdoppelt sich die Korrosionsrate pro 15 – 20 °C Temperatur.
Bei intermittierenden Anlagen kann die Korrosionsrate deutlich höher ausfallen. Wenn Mediumtemperaturen über 100 °C erreichen, bleibt die Dämmung zwar kälter, anstehendes Wasser verdunstet jedoch an der heißen Rohroberfläche und hinterlässt aggressive, salzige Rückstände. Bei jedem Temperaturwechsel und erneuter Zuwanderung von Feuchtigkeit schreitet die Korrosion fort.
Korrosionsschutz: Als Korrosionsschutz bezeichnet man Maßnahmen zur Vermeidung von Schäden, die durch Korrosion an metallischen Bauteilen hervorgerufen werden können. Da eine absolute Korrosionsbeständigkeit nicht erreicht werden kann, zielen die ergriffenen Schutzmaßnahmen im Allgemeinen darauf, die Geschwindigkeit des korrosiven Angriffs so weit zu verringern, dass eine Schädigung des Bauteils während seiner Lebensdauer vermieden werden kann.
Passiver Korrosionsschutz: Passiver Korrosionsschutz umfasst alle Maßnahmen, welche eine gegen korrosive Medien abschirmende Wirkung erzielen. Dies erreicht man u. a. durch einen geeigneten Überzug oder eine Beschichtung des Werkstoffes sowie konstruktive Maßnahmen (zum Beispiel Vermeidung von Wasseransammlungen, Überdachungen usw.). Beispiele für gegebenenfalls aktiv pigmentierte (z. B. Zinkstaub, -phosphat, früher auch Zinkchromat oder Bleimennige) Beschichtungsstoffe (d. h. flüssig, pastös oder pulverförmig aufgetragene Stoffe) sind Kunstharze (z. B. EP oder PU), Kunststoffe (z. B. PVC oder Kunststofffolien), Öle, Lack, Gummi oder Hartparaffine. Beispiele für (anorganische oder metallische) Überzüge sind eine Konversionsschicht durch eine Phosphatierung, eine Eloxalschicht, eine Harteloxalschicht, eine Chromatierung oder andere Umwandlungsschichten mit eher nichtmetallischem Charakter sowie Feuerverzinkungen, die ihrerseits wiederum eine schützende Passivierungsschicht ausbilden und darüber hinaus bei Beschädigung den Untergrund als Opferanode schützen.
Aktiver Korrosionsschutz mit Fremdstrom:
Eine weitere Möglichkeit für den kathodischen Korrosionsschutz kann mittels Fremdstrom und Fremdstrom-Anoden erreicht werden. Bei Erdöl-Pipelines werden dazu z. B. in Abständen von einigen Kilometern in einigen hundert Metern Abstand quer zur Leitung Elektroden im Boden versenkt, die mit einer Gegenspannung gespeist werden. Der andere Pol liegt an der Pipeline, so dass dieses Spannungsgefälle genau das galvanische Element aus Boden und Metallleitung ausgleicht, was sich konkret in der Größenordnung von wenigen Volt bewegt. Da dies von der chemischen Zusammensetzung des Bodens abhängt, muss dieser untersucht werden und die eingespeiste Gegenspannung an die örtlichen Gegebenheiten angepasst werden.
Aktiver kathodischer Korrosionsschutz ohne Fremdstrom:
Mit dem aktiven Korrosionsschutz ohne Fremdstrom verfolgt man das Ziel, ein Metall, das oft in Berührung mit beispielsweise Wasser kommt, vor Rost zu schützen. Hierzu bedient man sich eines unedleren Stoffes, der quasi für das Metall geopfert wird. Dazu wird ein Stromkreis aufgebaut, der aus der Redoxreaktion der Oxidation dieser Opferanode gespeist wird. Der Strom von wenigen Milliampere wird dabei über einen einfachen Stromkreis geführt.
Korrosionsarten:
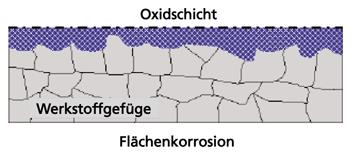
Flächenkorrosion: die betrifft die ganze Oberfläche eines Werkstücks oder Bauteils in gleichem Maß. Flächenkorrosion kommt nur bei Eisenmetallen vor, die nicht selbst eine schützende Oxidschicht bilden. Auch bei Edelstahl gibt es in der Regel keine Flächenkorrosion.
Erosionskorrosion:
Eine Erosionskorrosion (Kavitationskorrosion [punktuelle bzw. kleinflächige Abtragungen]) entsteht durch Kavitation und Implosionen an Engstellen (z. B. Rohrbögen, unentgratete Rohre, eingedrücke verengte Rohrquerschnitte) oder in Armaturen und Pumpen in Verbindung mit hohen Fließgeschwindigkeiten von Flüssigkeiten. Eine Erosion kann auch durch feste Stoffe (z. B. Sand) infolge eines Abriebes hervorgerufen werden.
Erosionskorrosion oder auch Kavitationskorrosion ist eine punktuelle bzw. kleinflächige Abtragung eines Metalls, die durch eine relativen hohe Fließgeschwindigkeit an einer Metalloberfläche entsteht. Es tritt häufig in Rohrbögen und Rohrengstellen (Eindellungen, Verschraubungen, nicht entgratete Schnittstellen) auf, die die Flussrichtung oder –geschwindigkeit beeinflussen bzw. erhöhen.

Spannungsrisskorrosion: ist ganz einfach die Korrosionsart, die am schnellsten zur Zerstörung des Stahls und zu Betriebsunterbrechungen führt. Außerdem ist die Spannungsrisskorrosion die Korrosionsart, die sich am schwierigsten reparieren lässt und damit auch die teuerste Korrosionsart. Kurz gesagt, ist die Spannungsrisskorrosion generell die folgenreichste aller Korrosionsarten und deswegen diejenige, die unter allem Umständen vermieden werden muss.

Spaltkorrosion: ist Lochfraß sehr ähnlich, beide werden häufig unter dem Begriff „örtliche Korrosion“ zusammengefasst. Der Unterschied besteht darin, dass Lochfraß auf freiliegenden Flächen auftritt, Spaltkorrosion hingegen in Spalten, Flanschenverbindungen, unter Schrauben, Gewinden, Poren und andere Engstellen ohne Konvektion oder andere Bewegungen, sodass Wasser still steht.
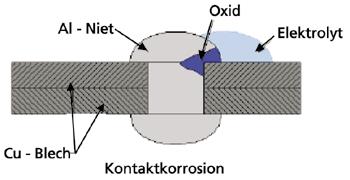
Kontaktkorrosion: entsteht, wenn zwei Metalle mit unterschiedlichem Lösungspotenzial durch einen Elektrolyt (Wasser, feuchte Luft …) leitend verbunden sind. Dabei wird das unedlere Metall zur Anode und das edlere zur Kathode. Diese zusätzliche Polarisierung führt zu einer beschleunigten Auflösung der Anode.
Beispiele: Schraube aus Kupfer in einem Aluminiumblech, Edelstahlblech mit Stahlblech verschraubt.
Lochfraßkorrosion: auch Lochkorrosion oder Lochfraß genannt, bezeichnet klein erscheinende Korrosionsstellen bzw. punktförmige Löcher in Oberflächen passivierter Metalle, die sich in der Tiefe trogförmig teils erheblich ausweiten. Lochfraßkorrosion bleibt wegen ihrer an der Oberfläche geringen Ausdehnung häufig lange unbemerkt.

Elektrochemische Korrosion:
Eine elektrochemische Korrosion findet immer dann statt, wenn ein Metall mit einer elektrisch leitenden Flüssigkeit (Elektrolyt) in Kontakt kommt.
Als Elektrolyt ist bereits eine dünne, adsorbierte Wasserschicht auf der Metalloberfläche ausreichend, die ab 70 bis 80% relativer Feuchte eine genügende Effizienz zur Auslösung elektrochemischer Korrosion hat, insbesondere durch gelöste Salze, Schwefeldioxid oder Kohlendioxid.
Die Elektrolytlösung besteht aus frei beweglichen, elektrisch geladenen Molekülbestandteilen – den positiven Kationen und den negativen Anionen, die sich gegenseitig elektrisch kompensieren müssen (Neutralitätsprinzip).
Die Reparatur von Korrosionsschäden: Welcher ist der richtige Zeitpunkt?
Bei jeder Reparatur spielen die Kosten eine wichtige Rolle. Es macht keinen Sinn, Unmengen an Ressourcen in die Reparatur eines Tanks aus nichtrostendem Stahl zu binden, wenn das Problem einige Monate später wieder auftritt. Wenn sich eine Kombination zwischen Stahl und Betriebsbedingungen nicht bewährt hat, müssen Änderungen bei Werkstoff und/oder Betrieb vorgenommen werden, damit eine Reparatur überhaupt Sinn macht. Wenn weder Stahl noch Betrieb optimiert werden, löst man das Problem nicht und es wird unweigerlich wieder Korrosion auftreten.
Reparatur von Korrosionsschäden, allgemeine Korrosion
Da sich eine allgemeine Korrosion durch eine gleichmäßige Verdünnung der Werkstoffstärke über große Flächen auszeichnet, sind etwaige Durchrostungen ein sicheres Anzeichen dafür, dass der restliche Stahl ebenfalls stark verschlissen ist. Die Anlage hat das Ende ihrer Lebensdauer erreicht und man kann guten Gewissens eine neue bestellen. Man sollte aber unbedingt das Allgemeinwissen insbesondere über allgemeine Korrosion von nichtrostendem Stahl nutzen und einen Stahl wählen, der eine längere Lebensdauer garantiert.
Reparatur von Korrosionsschäden, Lochfraß
Im Gegensatz zu allgemeiner Korrosion ist Lochfraß so lokal, dass es sich oft lohnt, die Korrosionsschäden zu reparieren und Änderungen im Betrieb vorzunehmen. Wertvolle Informationen kann man durch Untersuchen des Umfangs der Korrosion, aber auch der Stellen, an denen keine Korrosion erfolgt ist, gewinnen.
Letzteres liefert wertvolle Informationen, wie weit man davon entfernt ist, Korrosion vollständig zu vermeiden. Wenn die gesamte Ausrüstung stark von Lochfraß befallen ist, bleibt nur die Möglichkeit, die Ausrüstung zu verschrotten und eine neue zu bestellen. Bei einem begrenzten Ausmaß sind aber gewisse Erfolgschancen vorhanden.
Reparatur von Korrosionsschäden, Spaltkorrosion
Ist die Anlage nicht von Lochfraß befallen, weist dies auf eine ausreichende Güte des Stahls hin. Allerdings überschreitet die inhärente korrosionstechnische Schwächung durch Spalten die Korrosionsgrenze des Stahls. In diesem Fall kann man entweder die Spalten beseitigen oder falls dies möglich ist, eine selektive Verbesserung der Legierungsgüte an den kritischen Stellen.
Reparatur von Korrosionsschäden, Spannungsrisskorrosion
Spannungsrisskorrosion ist die Korrosionsform, die am schwierigsten zu reparieren ist. Natürlich ist der Versuch verführerisch, die Risse einfach durch Schweißen oder Flicken zu reparieren. Aber langfristig ist die keine Lösung. Selbst wenn der Flicken aus einem korrosionsbeständigeren Stahl besteht, muss dieser Flicken ja mit dem alten Stahl verschweißt werden. Und durch das Schweißen auf Stahl mit Spannungsrisskorrosion entstehen zahlreiche neue innere Zugsspannung. Diese inneren Spannungen führen zu einem Breiter werden von bisher unsichtbaren Rissen. Und selbst wenn trotz aller Widrigkeiten ein Schließen aller Risse gelingt, werden neue innere Zugsspannungen zu einer erneuten Spannungsrisskorrosion führen. Wenn unmittelbar nach den Reparaturen keine wesentlichen Änderungen in den Betriebsbedingungen erfolgen und insbesondere die Temperaturen sinken, stellt jede Reparatur eine Behelfslösung dar.
Beispiel für einen Korrosionsprozess: Ein einfacher Versuch zum Korrosionsschutz am Beispiel eines Eisennagels
1. Ein ungeschützter Eisennagel wird in angesäuertes Salzwasser gegeben. Nach einiger Zeit geht das Eisen in Lösung und korrodiert, da keine Opferanode vorhanden ist. Des Weiteren bildet sich Wasserstoff (H2) am Eisennagel.
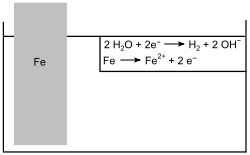
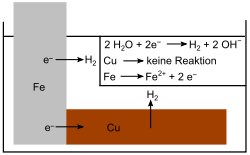
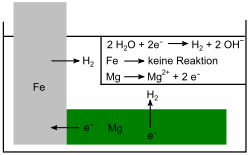
2. Der Eisennagel wird mit dem unedleren Magnesium geschützt. Es kommt zur Bildung eines Lokalelements, indem Magnesium (Mg) als Anode wirkt und sich somit für das Eisen (Fe) opfert. Es bildet sich Wasserstoff, also H2 an der Fe-Kathode. Der Grund hierfür ist im Elektronenfluss (e−) vom Mg zum Fe zu suchen, da Mg unedler ist als Eisen und somit ein größeres Reduktionsvermögen besitzt.
3. Beim Gegenversuch mit dem edleren Kupfer (Cu) wirkt das Eisen als Anode und das Kupfer kann das Eisen nicht vor der Korrosion schützen. Auffallend ist, dass das Eisen dadurch schneller oxidiert wird. Auch hierbei findet ein Elektronenfluss statt, der jedoch vom Fe zum Cu verläuft. Damit wird die Korrosion beschleunigt.